TERCERA UNIDAD
Na (Sodio)
El sodio es un elemento químico de símbolo Na, con número atómico 11, fue descubierto por Sir Humpry Davy. Es un metal alcalino blando, untuoso, de color plateado, muy abundante en la naturaleza, encontrándose en la sal marina y el mineral halita.
- Es muy reactivo, se oxida en presencia de oxígeno y reacciona violentamente con el agua.
- El sodio está presente en grandes cantidades en el océano en forma iónica, También es un componente de muchos minerales y un elemento esencial para la vida.
Características principales
- El sodio flota en el agua descomponiéndola desprendiendo hidrogeno y formando un hidróxido
Donde encontramos el sodio?
- Principalmente lo encontramos en la sal, pero está presente en todos los alimentos como un ingrediente natural o como un ingrediente añadido durante el proceso de elaboración. La principal fuente es la sal de mesa seguida de alimentos procesados, queso pan, cereales, carnes y pescados ahumados curados y en salmuera.
° Debido a que normalmente consumimos en exceso sodio, el problema es encontrar los alimentos que tengan menos cantidad. Estos alimentos son las frutas en general y en las verduras, que a su vez contienen más cantidad de potasio, el cual reduce en parte del excedente de sodio.
Sabías que el sodio...
Los tuaregs del desierto del Sahara tienen la sal como un bien muy preciado ya que, en poca cantidad, les ayuda a no eliminar demasiados líquidos a través del sudor evitando así deshidratarse.
Funciones extracelulares
A nivel extracelular los principales cationes son Na+ y K+, y los principales aniones Cl- y HCO3.
Las concentraciones de estos electrólitos afectan al metabolismo, al pH Intra y extracelular.
Además la diferente concentración de estos electro litros en los equipos intra y extra celulares, regula el funcionamiento del sistema nervioso y el tejido muscular. Las concentraciones de electro litros se pueden expresar de varias formas: miliequivalentes por litro = mEq/L. milimoles por litro = mmol/L.
PATOLOGIAS (ELEVACION Y DISMINUCION DEL SODIO)
HIPEPNATREMIA: se considera cuando la concentración de sodio en la sangre es mayor a 145 mEq/L. Las causas principales se deben a una vasopresina o ADH, a pérdidas excesivas de agua, y a un balance positivo de sal.
La presencia de trastornos neurológicos, aparecen con valores por encima de 160 mEq/L. que pueden caracterizarse por irritabilidad muscular, alteraciones del nivel de conciencia, coma e incluso convulsiones.
CAUSAS POR NIVELES ALTOS:
° Alta ingesta de sal en la dieta
° Sudoración
° Sed
° Diarrea, vómitos
° Insuficiente aporte de líquido
° Diabetes insípida
° Diabetes mellitus severa
° Quemaduras
HIPONATREMIA: se considera hiponatremia cuando la concentración de sodio en la sangre es menor a 135 mEq/L. Las causas principales incluyen: perdidas grandes de sodio (por uso diuréticos, diuresis osmótica o perdida de solutos a través de la orina que arrastran agua y sodio, enfermedades renales que aumenten la perdida de sodio urinario.
Se considera una disminución en la concentración de sodio por debajo de 125 mEq/L. es potencialmente fatal para el organismo humano.
CAUSAS POR NIVELES BAJOS:
° Ingesta baja de sodio
° Diarrea, vómitos
° Quemaduras
° Insuficiencia cardiaca
° Cirrosis hepática
° Insuficiencia renal con alto aporte de agua
° Insuficiencia suprarrenal (enfermedad de Addison)
° Medicamentos (incluyendo ciertos diuréticos, antidiabéticos, antidepresivos, fármacos cito tóxicos).
POTASIO (K)
Es un mineral esencial para nuestra dieta diaria útil al sodio y al cloro pertenece a la familia de los electrolitos
Es el principal catión intracelular un 98% del potasio corporal se encuentra en el interior de las células y solo un 2% es de extrema importancia en nuestro organismo

FUNCIONES
EXTRACELULAR:
Tres mecanismos son los responsables de mantener la concentración extracelular de K+ dentro de in estrecho margen
a) La permeabilidad para el potasio es alta en todas las células del organismo de forma que este catión es captado fácilmente a nivel celular y únicamente una pequeña fracción del potasio ingerido queda en el espacio extracelular
b) El epitelio del colon tiene capacidad para secretar potasio, lo cual va a estar estimulado cuando la capacidad renal de eliminación de potasio esta disminuida.
c) Los mecanismos renales residen en los túbulos distales y túbulos colaterales, juegan un papel clave y son los últimos responsables de responder de modo adecuado a cambios
INTRACELULAR
Regula el balance de agua y del ácido en la sangre y los tejidos. Las concentraciones en el interior son mayores que en exterior
Esta diferencia de concentraciones genera gradiente electroquímico conocido como potencial de membrana. Esto hace que el sodio se mueva hacia dentro de la célula y que el potasio se mueva fuera de la misma generando una potencia electro de membrana ayuda a generar las contracciones musculares
DONDE SE ENCUENTRA
FRUTAS:
-plátano
-melón
-naranja
-ciruela pasas
-uvas
VERDURAS
-papa
-calabaza
-espinaca
-camotes
-tomates
FRUTAS SECAS
-almendras
-nueces
-avellanas
-cacao
PATOLOGIAS
HIPERPOTASEMIA
Cuando esto sucede hay un mayor grado de excitabilidad celular y puede llegar a una excitación continua que puede dar una crisis exclusiva se puede producir por un fluido-terapia excesivamente rápido pero también cuando hay una insuficiencia renal
CALCIO
El calcio es un elemento químico, de símbolo Ca y de número atómico 20.
Características.
El calcio es un metal alcano terreo, arde con llama roja formando oxido de calcio. Las superficies recientes son de color blanco plateado pero presenta un cambio físico rápidamente, combinado, cambiando a un color levemente amarilla expuestas al aire y en última instancia grises o blancos por la formación de hidróxido al reaccionar con la humedad ambiental. Reacciona violentamente con el agua en su estado metal para formar Ca (OH)2 desprendiendo hidrogeno.
Ciclo esquelético.
El calcio esquelético o almacenado de los huesos, se distribuye entre un espacio relativamente no intercambiable, que es estable y del espacio rápidamente intercambiable, el cual participa en las actividades metabólicas. Se almacena principalmente en los extremos de los huesos largos y se moviliza para satisfacer el aumento de las necesidades de crecimiento, del embarazo y de la lactancia. En ausencia de dicha reserva ósea; si la ingesta inadecuada de calcio se prolonga, resulta en una estructura ósea deficiente.
Calcio Sérico.
Este calcio consta de 3 fracciones distintas: calcio libre o ionizado, calcio anicónico que se une a fosfato y calcio unido a proteínas, principalmente albumina o globulina. El calcio ionizado es el que realiza la mayoría de funciones metabólicas. Su concentración está controlada principalmente por la para horma, la calcitonina y la vitamina D. El calcio sérico se mantiene a niveles muy estrechos de 8,8 a 10,8 mg/dl.
Funciones.
Además de su función, en la construcción y mantenimiento de huesos y dientes, también afecta el transporte de las membranas celulares actuando como estabilizador de la membrana. Se requiere como en la transmisión nerviosa y en la regulación de los latidos cardiacos.
Deficiencia de Calcio.
Cuando la deficiencia es a largo plazo y desde etapas tempranas, puede causar:
-Deformidades óseas: entre ellas la osteomalacia, raquitismo, osteoporosis.
-La osteoporosis: fracturas con la más mínima tensión.
-La osteomalacia: desequilibrada coincidente en la captación de calcio y fosforo, incapacidad para mineralizar la matriz ósea, raquitismo, enfermedad relacionada con la malformación de los huesos en niños, los huesos no pueden sostener el peso y tensión ordinaria, que resultan piernas arqueadas y cosas así.
-Tetania: niveles muy bajos de calcio en sangre.
Requerimientos recomendados
Gpo/edad RDA
Lactante 6 meses 400 mg
6-12 meses 600 ||
1-10 años 800- 1200 mg
11-18 años 1200- 1500 ||
25-30 || 1000 (M)
800 (H)
Mujeres
Por menopaúsicas 1400-1500 mg
Cloro (Cl)
Elemento químico, símbolo Cl, de número atómico 17 y peso atómico 35.453. El cloro es uno de los cuatro elementos químicos estrechamente relacionados que han sido llamados halógenos. El flúor es el más activo químicamente; el yodo y el bromo son menos activos. El cloro reemplaza al yodo y al bromo de sus sales. Interviene en reacciones de sustitución o de adición tanto con materiales orgánicos como inorgánicos.

El cloro seco es algo inerte, pero húmedo se combina directamente con la mayor parte de los elementos.
Producción de cloro en las empresas.
El cloro es un gas altamente reactivo. Es un elemento que se da de forma natural. Los mayores consumidores de cloro son las compañías que producen dicloruro de etileno y otros disolventes clorinados, resinas de cloruro de polivinilo (PVC), clorofluorocarbonos (CFCs) y óxido de propileno. Las compañías papeleras utilizan cloro para blanquear el papel. Las plantas de tratamiento de agua y de aguas residuales utilizan cloro para reducir los niveles de microorganismos que pueden propagar enfermedades entre los humanos (desinfección).
Reacción del cloro en el organismo.
La exposición al cloro puede ocurrir en el lugar de trabajo o en el medio ambiente a causa de escapes en el aire, el agua o el suelo. El cloro entra en el cuerpo al ser respirado el aire contaminado o al ser consumido con comida o agua contaminadas. No permanece en el cuerpo, debido a su reactividad. Los efectos del cloro en la salud humana dependen de la cantidad de cloro presente, y del tiempo y la frecuencia de exposición. Los efectos también dependen de la salud de la persona y de las condiciones del medio cuando la exposición tuvo lugar.
Efectos ambientales del Cloro.
El cloro se disuelve cuando se mezcla con el agua. También puede escaparse del agua e incorporarse al aire bajo ciertas condiciones. La mayoría de las emisiones de cloro al medio ambiente son al aire y a las aguas superficiales.
Una vez en el aire o en el agua, el cloro reacciona con otros compuestos químicos. Se combina con material inorgánico en el agua para formar sales de cloro, y con materia orgánica para formar compuestos orgánicos clorinados.
Debido a su reactividad no es probable que el cloro se mueva a través del suelo y se incorpore a las aguas subterráneas.
Las plantas y los animales no suelen almacenar cloro. Sin embargo, estudios de laboratorio muestran que la exposición repetida a cloro en el aire puede afectar al sistema inmunitario, la sangre, el corazón, y el sistema respiratorio de los animales.
Se encuentra comúnmente en: la sal común, algas, aceitunas, agua del grifo.
Función en el organismo.
El cloro se encuentra en los líquidos extracelulares de nuestro organismo. La mayor parte de cloro en nuestro organismo es aportado por la sal de cocina.
El cloro permite el buen funcionamiento del hígado, la producción de los jugos gástricos y el mantenimiento de los huesos. Está también muy a menudo en relación con el Sodio y el Potasio. La función de estos tres es de:
- Repartir el agua a nuestro organismo.
- Regular la presión osmótica (equilibrio entre los líquidos extracelulares e intracelulares).
- Participar en la neutralidad eléctrica del organismo.
- Mantener el equilibrio ácido-base.
- Favorecer el transporte del CO2 en la sangre.
Valores normales.
En los hombres, en las mujeres y en los niños, el valor normal del cloro en la sangre es el mismo. Debe encontrarse entre 100 y 105 mmol/L.
Cloro bajo.
El nivel de cloro puede disminuir si se trata de una hipocloremia. Una hipocloremia, raramente, se trata de una carencia en aportaciones. Por lo general, es una consecuencia de una disfunción:
- Diarreas
- Vómitos prolongados
- Transpiración excesiva
Los primeros síntomas de una hipocloremia son:
- Cansancio
- Calambres musculares
- Agitación
- Tetania
- Trastorno del ritmo cardíaco
Cloro alto.
El nivel de cloro en la sangre aumenta en muy raras ocasiones. De hecho, cuando el organismo contiene demasiado cloro, es eliminado por las orinas.
Cuando ciertas disfunciones causan una hipercloremia, los primeros síntomas son:
- Respiración rápida y profunda
- Debilidad muscular
- Vómitos
- Destrucción de la flora intestinal
FOSFORO (P) |
El fósforo es un elemento químico de número atómico 15 y símbolo P.
El fósforo es un mineral que está muy presente en nuestro organismo, y que puede adquirirse sin problemas a través de una dieta sana. El fósforo es, junto el calcio, el principal componente de los huesos.

Fue descubierto por el alquimista alemán Hennig Brandt en 1669 en Hamburgo al destilar una mezcla de orina y arena (utilizó 50 cubos) mientras buscaba la piedra filosofal.
¿DÓNDE ENCONTRAMOS EL FOSFORO?
El fósforo está en todo nuestro alrededor. Está presente en pequeñas concentraciones en los océanos, lagos, mares y ríos. El fósforo es esencial para la vida. Es parte de las rocas y los minerales del suelo. El fósforo es el segundo nutriente mineral más abundante en el cuerpo humano, solo superado por el calcio. Representa más del 20% de total de minerales en el cuerpo. Cerca del 80% del fósforo se encuentra en los huesos y dientes. El resto está ampliamente distribuido en todo el cuerpo combinado con las proteínas, grasas y sales de cada célula viva.
Al encontrarse en la mayoría de los alimentos, solo mencionaremos los que contienen más de 0,4 g. por cada 100 g.
Frutos secos: girasol, sésamo, pistacho, almendras.
Legumbres: soja, alubias, garbanzos y lentejas.
Cereales: trigo, copos de avena, arroz integral, levadura, salvado de trigo.
FUNCIONES
- Función extracelular
El fosfato inorgánico representa la fuente de fosfato sanguíneo para huesos y dientes y forma parte del sistema tampón del pH de la sangre. El fosfato orgánico, por otra parte, es una parte importante de la célula, tanto a nivel de la membrana plasmática como integrado en moléculas de la importancia del ATP, el AMPc o los ácidos nucleicos. En la regulación de los niveles orgánicos de calcio y fósforo intervienen, fundamentalmente, la parathormona u hormona paratiroidea, la calcitonina y la vitamina D.
- Función Intracelular
Hiperfosfatemia
El fósforo total de nuestro organismo es de unos 700 g, de los que el 80-90 % se localiza a nivel óseo, un 10-14 % está en el interior de las células y un 1 % tiene una localización extracelular.
Definimos la hiperfosfatemia como las cifras de fósforo en sangre superiores a 5 mg/dl en los adultos o 7 mg/dl en los niños. Afecta por igual a ambos sexos y no existen diferencias de razas. Es más frecuente en ancianos debido a que la incidencia de insuficiencia renal crónica, principal causa de la hiperfosfatemia, se incrementa con la edad. Si es importante y aguda determina hipocalcemia y tetania. En los casos crónicos puede ocasionar calcificaciones vasculares y tisulares, especialmente en situaciones de insuficiencia renal.
AUMENTO DEL FOSFORO
Acidosis metabólica: la acidosis favorece la descomposición de compuestos intracelulares que contienen fósforo; hay pérdida neta de fósforo intracelular que se pierde por la orina; cuando el organismo se recupera de la acidosis se produce hipofosfatemia.
- Diabetes: la diuresis osmótica (aumenta la excreción renal de fósforo), la acidosis metabólica por cetoacidosis y administración de insulina favorecen la hipofosfatemia.
- Alcoholismo: la intoxicación aguda por alcohol y el alcoholismo crónico producen hipofosfatemia con gran frecuencia (30% de los alcohólicos ingresados)
- Cirugía: sobre todo si es del tracto gastrointestinal y si se sigue de la administración de soluciones de glucosa.
DISMINUCION DEL FOSFORO
La disminución de fósforo en el cuerpo ocurre por alcoholismo, sobredosis de antiácidos o barbitúricos, glucosa intravenosa y deficiencia de vitamina D. Cuando una persona se vuelve fósforo deficiente desarrolla debilidad muscular, anemia e incrementa la sensibilidad a las infecciones. Si una persona necesita phosphorus es útil evaluar si hay algunos factores en ella o en su vida que le esté causando una sobre dosis de fósforo o una fósforo deficiencia.
VALORES NORMALES
Los valores normales van de 2.4 a 4.1 miligramos por decilitro (mg/dL).
Los ejemplos de arriba son mediciones comunes para los resultados de estos exámenes. Los rangos de los valores normales pueden variar ligeramente entre diferentes laboratorios. Algunos laboratorios utilizan diferentes mediciones o analizan muestras diferentes. Hable con el médico acerca del significado de los resultados específicos de su examen.
Significado de los resultados anormales
Los niveles por encima de lo normal (hiperfosfatemia) pueden deberse a muchas afecciones médicas diferentes. Las causas comunes abarcan:
- Cetoacidosis diabética
- Hipoparatiroidismo
- Demasiado fosfato en la alimentación
- Enfermedad hepática
- Insuficiencia renal
- Demasiada vitamina D
Uso de ciertos medicamentos como laxantes que contengan fosfato
Los niveles por debajo de lo normal (hipofosfatemia) pueden deberse a:
- Alcoholismo
- Hipercalcemia
- Hiperparatiroidismo
- Desnutrición grave
Muy poca ingesta de fosfato o Vitamina D en la dieta, lo que ocasiona raquitismo (niñez) u osteomalacia (adultez).
ENFERMEDADES EN LAS CUALES SU USO PUEDE HACERSE ACONSEJABLE:
Estas son algunas de las enfermedades en las que el uso del fosforo, puede estar indicado:
Corazón/ Cardiología: Taquicardias, trastornos del musculo cardiaco.
Traumatología/ Reumatología: Artritis Artrosis Espondiloartritis anquilosante Raquitismo Reuma Sinovitis toxica
Trastornos del metabolismo: Alteraciones del colesterol o triglicéridos
Estomatología: Caries, Encías sangrantes, Gingivitis, Piorrea, Trastornos de la dentición.
Riñón/ Urología: Trastornos renales.
Sistema nervioso/ Neurología: Ansiedad Angustia Depresión Estrés
Otros:
- Anorexia
- Esclerosis múltiple
- Falta de calcio
- Fatiga mental o física
- Hipotiroidismo
- Infertilidad masculina
- Insuficiencia en la secreción de leche materna
- Temblores
- Retraso de crecimiento
- Uso de antiácidos
TECNICA DEL SODIO
Anteriormente al fotómetro de flama y los electrodos ion-selectivos, el método más popular para determinar sodio en los fluidos corporales involucran su precipitación como una sal triple de acetato de zinc uranilo sódica. El método presentado es esencialmente una adaptación del último esquema, en donde el sodio se precipita del sobrenadante libre de proteínas como triple sal. La disminución resultante de la absorbancia de la mezcla de reactivo de color-sobrenadante es proporcional al contenido de sodio de la muestra.
REACTIVOS
Reactivo de Color de Sodio.
Solución de acetona de uranilo, 5.3g/dL y acetato de zinc, 15.4g/dL, en solución acuosa acido acético-etanol.
Reactivo precipitante.
Solución acuosa de acido tricloroacetico (TGA), 10g/dL.
Estándar de sodio.
Cloruro de sodio de 140mmol/L, en solución TCA. Equivalente a un valor de sodio de 140mmol/L cuando se utiliza como se indica en este método.
MATERIALES REQUERIDOS:
*Espectrofotómetro capaz de leer absorbencias a 420 nm.
*Centrifuga con alta capacidad de velocidad (>1500 rpm)
*Pipetas exactas de 0.5 y 2.5 mL.
*Tubos de prueba y celdillas.
*Agitador.
* Vortex.
*Cronómetro.
PROCEDIMIENTO
Preparación del sobrenadante libre de proteínas.
1. Añada 0.5 ml de suero plasma u orina diluida a tubos adecuadamente marcados
2. Añada 0.5 ml de reactivo precipitante gota a gota a cada tubo con agitación vigorosa
3. Dejelo reposar por 5 minutos después centrifugue
Procedimiento
1. Pipetee en los tubos marcados los siguientes volúmenes (mL), agitando rápidamente después de cada adición del reactivo de color
|
|
Reactivo Blanco (RB) |
Estándar (S) |
Muestra (U) |
|
Agua Destilada |
0.5 |
|
|
|
Estándar |
|
0.5 |
|
|
Sobrenadante |
|
|
0.5 |
|
Reactivo color |
2.5 |
2.5 |
2.5 |
2. Nuevamente mezcle el contenido de todos los tubos
3. Incube los tubos por 10 minutos a temperatura ambiente (15 – 25°C)
4. Después de incubar, mezcle y centrifugue a alta velocidad por 5 min
5. Transfiera con cuidado el sobrenadante de cada tubo en la celdilla apropiada
6. Con el espectofotometro a 420nm. Lea y registre absorbancia del blanco reactivo, estándar y de la muestra en 30 min
RESULTADOS
Los valores se derivan del siguiente calculo:
Sodio en suero, plasma u orina (mmol/L)
Abs(RB)- Abs (U) X140
Abs( RB)- Abs (8)
Donde Abs (RB) Abs (U) y Abs (8) representan las absorbancias del blanco del reactivo , muestra y estándar respectivamente, y 140 es el valor equivalente del estándar del sodio en mmol/L
NOTA: Los valores de orina se deben multiplicar por el factor de
dilución apropiado.
Sodio en orina (mmoI/24 h) =
Sodio en orina (mmol/L) x volumen de 24 h (mL)
1000
VALORES ESPERADOS
Rango normal: Suero/plasma 135 – 155 mmoI/L
Orina 75 – 200 mmoI/24h
TECNICA DEL POTASIO
El método presentado para la determinación de potasio se basa en la técnica turbidimetrica publicada por Hillman y Beyer en 1967. Los resultados coincidían favorablemente con aquellos obtenidos por fotometría de flama y fueron adecuados para la detección rápida de híper e hipokalemia en ausencia de un fotómetro de flama o electrodo ion-selectivo. Los iones potasio en un medio alcalino libre de proteínas reaccionan con el tetrafenilborato de sodio para producir una suspensión turbia finamente dispersa de tetrafenilborato de potasio. La turbidez producida es proporcional a las concentraciones de potasio.
REACTIVOS
-Reactivo de borato de potasio.
Solución acuosa de tetrafenilborato de sodio, 0.2 moI/L
-Reactivo de hidróxido de Sodio.
Hidróxido de sodio acuoso, 2.0 moI/L
-Reactivo de TCA Precipitante.
Solución acuosa de ácido tricloroacético (TCA) 0.3 moI/L
-Estándar de Potasio (Equivalente a 4.0 mmoI/L).
Solución de cloruro de potasio en TCA acuoso (0.3 moI/L)
MATERIAL REQUERIDO
*Espectrofotómetro capaz de leer absorbancias a 580 nm
*Centrifuga
*Pipeta automática de 0.1, 0.2, 1.0, 2.0, y 9.0 mL.
*Vasos graduados, probetas o pipetas.
*Tubos de prueba o celdillas
*Agitador vortex
*Agitador
PROCEDIMIENTO
Preparación del sorbrenadante de libre de proteínas.
1. Añada 0.05 mL de suero, plasma u orina diluida a tubos
Previamente etiquetados.
2. Añada 0.5 mL de Reactivo TCA precipitante gota a gota a
Cada tubo mezclado vigorosamente (de preferencia utilizar
vortex).
3. Déjelo por 5minutos, después centrifugue a alta velocidad por
5 – 10 minutos.
Procedimiento de la prueba
1. Añada el estándar o el sobrenadante claro en la mitad de la
Superficie del reactivo de trabajo, asegúrese que cada
Celdilla sea mezclada con cuidado antes de proseguir con la
Siguiente muestra, de acuerdo al siguiente esquema:
Nota: Puede utilizar todos los volúmenes al doble si el
Instrumento que utiliza requiere volúmenes mayores a 1.0 mL.
1. Incube todas las celdillas a temperatura ambiente por 5
Minutos.
2. Lea S y U contra RB a 580 en un intervalo de 60 minutos.
Control de calidad: En cada corrimiento de muestras se debe
Incluir un control de suero y/u orina ensayados ya sea por este
Método, fotómetro de flama o electrodo ión selectivo.
RESULTADOS
Los valores se pueden derivar por la siguiente ecuación:
Potasio en suero, plasma u orina (mmoI/L)=Au x 4
As
Orina Potásica (mmol/L x Volumen de 24 h (mL)
1000
Donde Au y As son los valores de absorbancia de la muestra y
Estándar, respectivamente, y 4 es la concentración del estándar.
VALORES ESPERADOS
Rango Normal: Suero 3.6-5.5 mmol/L
Plasma 3.5-4.8 mmol/L
Orina 26-123 mmol/24h (varía con la dieta).
TECNICA DEL CALCIO
Medición del calcio en suero:
En una solución muy alcalina, el calcio forma una calceína un complejo que presenta una intensa fluorescencia verde amarillenta bajo la luz ultravioleta de gran longitud de onda.
Método:
1. La micro cubeta se llena de solución de EDTA. Se preparan tres cubetas de plástico para titulación, con el siguiente contenido:
Blanco: 0.020 ml de agua sin iones.
0.10 ml de solución de KOH 1.25 N.
0.010 ml de solución de calceína.
Patrón: igual que el blanco pero con 0.020 ml de solución patrón de calcio en lugar de agua.
Problema: como el blanco pero con 0.020 ml de suero en lugar de agua.
2. Las tres cubetas se titulan sucesivamente, bajo una lámpara de ultravioletas de gran longitud de onda, de 100 watios, si es posible en un lugar obscuro
Determinacion de cloruros por valoracion mercurimetrica
Objetivo:
Realizar la determinacion de iones cloruros en suero por valoracion mercurimetrica (Metodo de Schales y Shales modificado) con nitrato de mercurio en presencia de difenilcarbazona como indicador.
Introduccion:
El ion del cloruro es el principal anión extracelular con 103 mEq/L de la concentración total de aniones que es de 154 mEq/L. Interviene de modo muy importante en el mantenimiento de la hidratación y la presión osmótica apropiadas y del balance anion-cation de este mismo comportamiento.
Fundamento:
Los iones de cloruro del seuro se titulan con una solucion valorada de nitrato de mercurio en presencia del indicador difenilcarbazona. Los iones Hg++ se combinan con los iones Cl- para formar soluble no ionizado, el exceso de Hg++ que no reacciono con los iones clouros se combina con el indicador difenilcarbazona para formar un complejo de color violeta azulado.
Reaccion:
Hg++ +
Hg++ + Difenilcarbazona Complejo color violeta azuldo
Material:
· Equipo para la toma de muestra
· Perrilla para pipetear
· Gradilla
· Tubos de ensayo
· Balanza analitica
· Muetra: suero sanguineo
Reactivos:
1. Solucion de difenilcarbazona (1mg/ml): Disolver 50 mg de difenilcarbazona en 50 ml de alcohol etilico, agitar y usar.
2. Solucion de nitrato de mercurio (0.015N). pesar 3 gr de nitrato de mercurio monohidratado y disolverlos en 300 ml de agua destilada. Agregar inmediatamente 2.6 ml de acido nitrico y aforar a 1000ml.
3. Agua destilada
4. Solucion estandar para cloruros
Procedimiento:
|
Reactivos: |
Estándar (100mEq/L): |
Problema (paciente): |
|
1-Suero |
--------------- |
0.2 ml suero |
|
2-Estandar de cloruros |
0.2 ml de estándar |
----------------- |
|
3-Agua destilada |
1.8 ml de agua destilada |
1.8 ml de agua destilada |
|
4-Difenilcarbazona |
0.6ml |
0.6ml |
|
5-Nitrato de mercurio |
Fracción de 0.01ml*** |
Fracción de 0.01ml*** |
***Mezclar y continuar añadiendo nitrato de mercurio hasta la aparición de color violeta azulado.
Calculos:
Concentracion de cloruros= volumen de Hg(NO3)2 utilizado para titular de la muestra (en ml) X100
(en mEq/L) Volumen de Hg(NO3)2 utilizado para titular el estandar (en ml)
Valores normales de cloruros en suero. 96 a 16 mEq/L
Técnica del Fosforo inorgánico:
El fosforo inorgánico reacciona con el molibdato de amonio en presencia de acido sulfúrico para producir un complejo de fosfomolibdato no reducido. El incremento de la absorbancia a 340nm es directamente proporcional a la concentración de fosforo inorgánico en la muestra.
Recolección y preparación de la muestra:
La muestra de elección deberá ser un suero fresco, claro y no hemolizado. Las muestras podrán guardarse hasta 7 días a una temperatura de 2-8ºC y hasta por 6 meses a una temperatura de -20 a 0ºC.
Preparación del reactivo:
El reactivo de trabajo se prepara combinando los volúmenes iguales del reactivo de molibdato de fosforo y del reactivo catalizador del fosforo. Bien mezclado antes de usarlos.
Materiales:
· Reactivo de trabajo.
· Un anazador que sea capaz de leer la absorbancia con exactitud.
· Cubetas de 1 cm o una celda de flujo que transmita luz a 340nm.
· Tubos de ensayo del tamaño adecuado.
· Pipetas del tamaño adecuado.
· Agua des ionizada.
· Un cronometro apropiado.
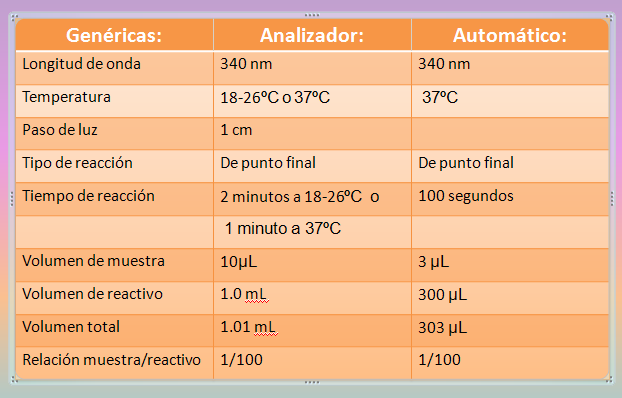
Procedimiento:
· Prepare el volumen requerido de reactivo de trabajo de fósforo.
· En tubos de ensayo por separado, pipetee 10 µL de agua des ionizada, estándar de fosforo o del suero a ser analizado.
· Agregue 1.0 mL del reactivo de trabajo del fosforo y mezcle.
· Incube la mezcla por 2 minutos a una temperatura de 18-26ºC, por un minuto a 37ºC. Determine la absorbancia del estándar (As) y de cada suero (A) a 340nm utilizando la muestra de agua des ionizada como blanco de reactivo.
Cálculos & Resultados:
Fosforo en mmol/L (mg/dL)= x concentración del estándar.
![]() A= absorbancia de la muestra desconocida.
A= absorbancia de la muestra desconocida.
![]() AS= absorbancia del estándar.
AS= absorbancia del estándar.
La concentración del fosforo inorgánico se expresa en mmol/L (mg/dL).
Valores esperados:
0.97- 1.45 mmol/L (3.0-4.5mg/dL). Se sugieren estos valores como referencia. Se recomiendan que cada laboratorio establezca el rango normal para el área en que está localizado.
